Analytisches CRO für die Life Science Industrie
ANALYTISCHES CRO FÜR BIOANALYTIK UND QUALITÄTSKONTROLLE
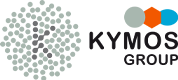
Die Kymos Group ist ein analytisches CRO mit drei europäischen Laboren, die sich der Bereitstellung bioanalytischer und CMC-Lösungen während des gesamten Produktlebenszyklus widmen: von der frühen Forschung und Entwicklung bis hin zur Herstellung und Vermarktung. Wir sind GLP- und GMP-zertifiziert, wurden erfolgreich von der EMA und der FDA inspiziert und sind Experten für Quatliätskontrolle von Small Molecules, Biologics und Nukleinsäuren. Wir bieten Dienstleistungen für Kunden der Pharma-, Biotechnologie-, Veterinär-, Feinchemie-, Kosmetik- und Nahrungsergänzungsmittelindustrie an. Unsere GMP/GLP-zertifizierten bioanalytischen und CMC-Dienstleistungen sind in folgende Bereiche unterteilt:
Bioanalytik Small Molecules
Entwicklung und Validierung unter GLP von bioanalytischen Methoden für Innovatoren und Generika mittles LC-MS/MS. Wirkstoffbestimmung in biologischen Proben aus präklinischen und klinische n Studien, PK/PD Evaluierung und Bioverfügbarkeits- und Bioequivalenzstudien.
Bioanalytik Biologics
Entwicklung und Validierung unter GLP von bioanalytischen Methoden für Innovatoren und Generika mittles ELISA, ECLA oder LC-MS/MS und Anti-Drug-Antibodies Bestimmung (ADAs) mit Bindungs- und Neutralisierungsassays. Wirkstoffbestimmung in biologischen Proben aus präklinischen und klinische n Studien und PK/PD Evaluierung.
Enzymaktivitätsbestimmung
Enzymaktivitätstests unter GLP/GMP-Bedingungen sowohl in bioanalytischen als auch in CMC-Projekten für natürliche und künstlich hergestellte Enzyme, enzymatische Biomarker und Enzyminhibitoren in biologischen Proben und Formulierungsproben.
Analytik von Nukleinsäuren
Analyse von DNA- und RNA-basierten Biomarkern, therapeutischen Oligonukleotiden, Impfstoffen und Spezialarbeiten mit mRNA, microRNA, siRNA, Aptameren und AntagomiRs mittels Real Time qPCR (RTqPCR), LC-MS/MS und Hybridisierungs-ELISA-Plattformen unter GLP.
Qualitätskontrolle Small Molecules (physikalisch-chemische Analyse)
GMP-zertifizierte Qualitätskontrolle für Small Molecules wie Rohstoffe, APIs, Hilfsstoffe, Zwischenprodukte, IMPs, Fertigprodukte, Verpackungsmaterialien, Herstellungsausrüstung und Prozessumgebungsproben gemäß den Kundenspezifikationen oder den einschlägigen Pharmakopöen (EP, USP, BP, JP)
Qualitätskontrolle Biologics (biopharmazeutische Tests)
Komplexe Charakterisierungen innovativer Biologika, Bewertungen der Biosimilarität und routinemäßige Chargenprüfungen und Freigaben für Biopharmazeutika nach GMP. EMA and FDA inspiziert.
Freigabeanalytik und Qualified Person
GMP-zertifizierte Dienstleistungen für Import, Chargenprüfung und Chargenfreigabe. Wir verfügen über mehrere QPs und sind zertifizierte Importeure und Hersteller (MIA-Inhaber) für die Qualitätskontrolle und Chargenzertifizierung von Human-, Tier- und Prüfarzneimitteln (IMPs), mit der Möglichkeit, sterile, nicht sterile und biologische Arzneimittel freizugeben
Stabilitätsstudien
GMP-zertifizierte ICH-Stabilitätsstudien und laufende Stabilitätsstudien für kleine oder große Moleküle in Fertigprodukten, von Tabletten, Kapseln und Ampullen bis hin zu topischen Produkten, Injektionsmitteln und Pulvern. Unsere beiden EU-Standorte verfügen über begehbare Klimakammern mit einer Lagerkapazität von insgesamt 100 m3 für die ICH-Zonen II, IVb und zusätzliche Bedingungen.





DG-GT Meeting: Dresden, DE | 10-11 Mar 2025
BIO CHINA 2025: Suzhou, CHN | 13-15 Mar 2025
BIO-Europe Spring: Milan, IT | 25-26 Mar 2025
German Pharm-Tox Summit: Hannover, DE | 25-28 Mar 2025
German Biotech Days: Heidelberg, DE | 09-10 Apr 2025
MEET2WIN: Bourdeaux, FR | 06-07 May 2025
BIO KOREA 2025: Seoul, KR | 07-09 May 2025
BIONNALE 2025: Berlin, DE | 14-15 May 2025
Innovation for Cell and Gene Therapies (ICGT): Paris, FR | 22 May 2025
MabDesign Partnering Day: Lyon, FR | 02 Jun 2025
Congrès Polepharma Biotesting: Evreux, FR | 04-05 Jun 2025
International Oligonucleotides and Peptides Conference: Prague, CZ | 09-11 Jun 2025
AFI Simposio: Rimini, IT | 11-13 Jun 2025
Antibody Industrial Symposium (AIS): Tours, FR | 25-26 Jun 2025
CPHI 2025: Frankfurt, DE | 28-30 Oct 2025