El Grupo Kymos cuenta con un equipo especializado y dedicado enfocado en el desarrollo y validación de métodos de prueba para productos medicinales de terapia génica, específicamente vectores virales como el virus adenoasociado (AAV), el adenovirus (AdV) y el lentivirus (LV).
Nuestros laboratorios cuentan con las certificaciones GLP y GMP, y son inspeccionados por la EMA y la FDA. Ofrecemos un servicio integral de control de calidad en un entorno regulado y validado, apoyándole en todas las fases, desde el descubrimiento de fármacos hasta la aprobación de comercialización, acelerando así la comercialización de productos de terapia génica.
Equipados con tecnologías y técnicas de vanguardia para garantizar la mejor calidad y optimizar los plazos, como qTOF-MS, SEC y HPLC AEX, CE-LIF, icIEF, qPCR y ELISA, ofrecemos un catálogo completo de ensayos precalificados por CMC para vectores virales. Esta combinación de científicos especializados y técnicas avanzadas nos permite adaptar nuestros métodos implementados o desarrollar nuevos según las necesidades específicas de cada estudio.
SERVICIOS
Servicios de análisis de vectores virales
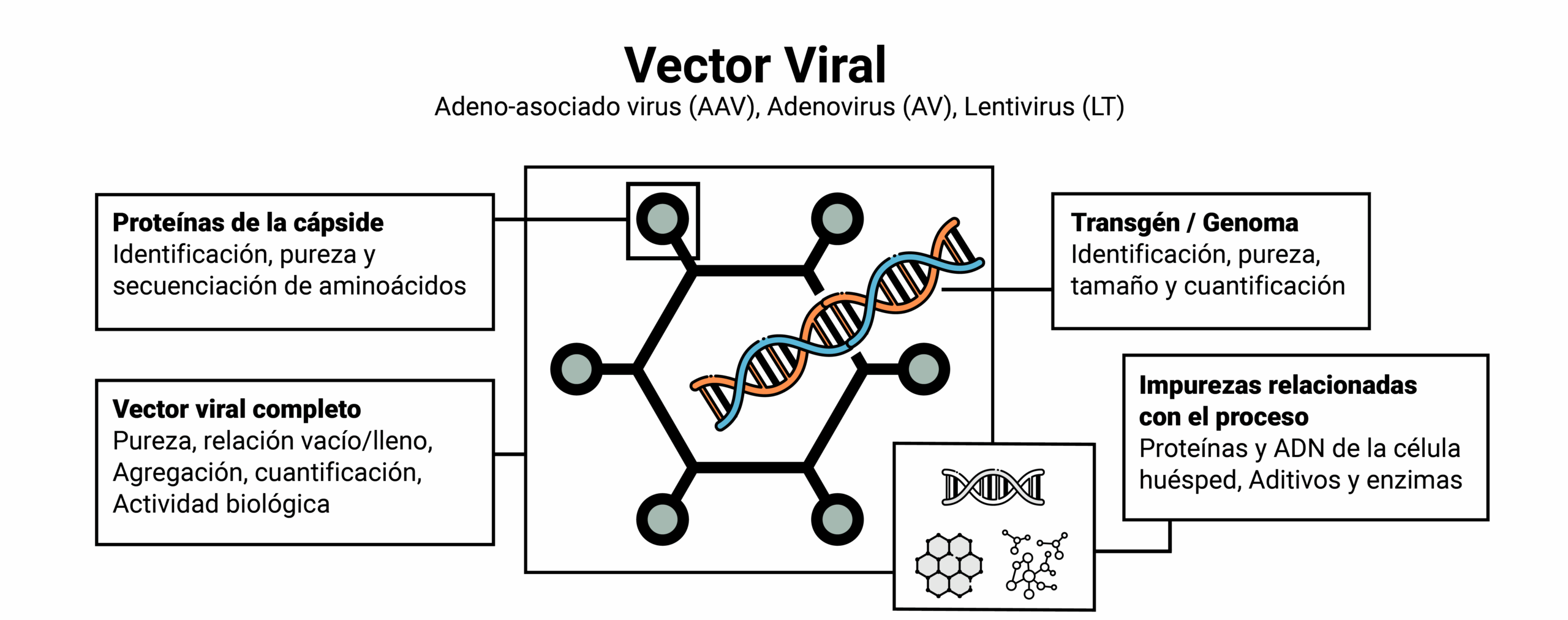
Caracterización de las proteínas de la cápside
La cápside de los vectores virales está compuesta por proteínas. Su integridad e identidad deben evaluarse mediante técnicas comunes de caracterización proteica. En Kymos Group, ofrecemos los siguientes ensayos:
- Determinación del peso molecular de los componentes proteicos mediante cromatografía líquida acoplada a espectrometría de masas de alta resolución (LC-HRMS)
- Relación correcta de los componentes proteicos de la cápside y pureza mediante electroforesis capilar en gel (ECG)
- Relación correcta de los componentes proteicos de la cápside y pureza mediante SDS-PAGE
- Secuenciación de aminoácidos de las proteínas de la cápside mediante digestión enzimática y análisis LC-MS/MS
Caracterización del transgén/genoma
El transgén o genoma del vector viral que contiene la información que debe transferirse a las células diana debe caracterizarse adecuadamente y su pureza e identidad deben determinarse. Kymos desarrolla los siguientes ensayos:
- Identidad de tamaño y pureza mediante electroforesis capilar en gel con fluorescencia inducida por láser (GCE-LIF)
- Secuenciación de nucleótidos transgénicos e impurezas de ADN mediante NGS (en desarrollo con un socio)
- Cuantificación de transgenes mediante qPCR (en desarrollo)
- Cuantificación total de ADN mediante métodos de fluorescencia
Caracterización completa del vector viral
Es necesario determinar los atributos de calidad del vector viral para garantizar la seguridad y eficacia de cada lote fabricado. En Kymos se pueden evaluar varios atributos de calidad:
- Cuantificación, relación cápsides vacías/llenas y pureza mediante cromatografía de intercambio aniónico (AEX)
- Cápsides vacías/llenas y agregación mediante microscopía electrónica de transmisión (MET) (en desarrollo con un socio)
- Agregación por cromatografía de exclusión por tamaño (SEC)
- Cuantificación por ELISA
- Actividad biológica, expresión de proteínas
Análisis de impurezas relacionadas con el proceso
Las impurezas relacionadas con el proceso pueden tener estructuras químicas muy diversas: ácidos nucleicos, proteínas, moléculas pequeñas, etc. Kymos dispone de una amplia gama de herramientas analíticas para el análisis de esta amplia gama de compuestos. Algunos ejemplos son:
- Proteínas residuales de células huésped mediante ELISA
- ADN residual de células huésped y plásmidos mediante qPCR (en desarrollo)
- Tamaño del ADN residual de la célula huésped para lentivirus mediante gel capilar
- Electroforesis con fluorescencia inducida por láser (GCE-LIF)
- Enzimas residuales como la benzonasa por ELISA
- Antibióticos residuales por HPLC

¿Por qué elegir KYMOS?
Servicios
Servicios relacionados con la Caracterización de Vectores Virales
Contacto




